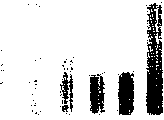CN1131712C - 初乳肽及其用途 - Google Patents
初乳肽及其用途 Download PDFInfo
- Publication number
- CN1131712C CN1131712C CN97198535A CN97198535A CN1131712C CN 1131712 C CN1131712 C CN 1131712C CN 97198535 A CN97198535 A CN 97198535A CN 97198535 A CN97198535 A CN 97198535A CN 1131712 C CN1131712 C CN 1131712C
- Authority
- CN
- China
- Prior art keywords
- colostrinin
- medicine
- treatment
- application
- disease
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 108010002212 colostrinine Proteins 0.000 title claims abstract description 157
- 239000003814 drug Substances 0.000 claims abstract description 30
- 208000024827 Alzheimer disease Diseases 0.000 claims description 16
- 206010036631 Presenile dementia Diseases 0.000 claims description 13
- 241000282414 Homo sapiens Species 0.000 claims description 12
- 208000015114 central nervous system disease Diseases 0.000 claims description 10
- 238000002360 preparation method Methods 0.000 claims description 10
- 208000028017 Psychotic disease Diseases 0.000 claims description 6
- 230000001684 chronic effect Effects 0.000 claims description 5
- 206010012289 Dementia Diseases 0.000 claims description 4
- 230000004770 neurodegeneration Effects 0.000 claims description 4
- 208000015122 neurodegenerative disease Diseases 0.000 claims description 4
- 108010020048 valyl-glutamyl-seryl-tyrosyl-valyl-prolyl-leucyl-phenylalanylproline Proteins 0.000 claims description 3
- 208000026072 Motor neurone disease Diseases 0.000 claims description 2
- 208000005264 motor neuron disease Diseases 0.000 claims description 2
- 201000001119 neuropathy Diseases 0.000 claims description 2
- 230000007823 neuropathy Effects 0.000 claims description 2
- 208000033808 peripheral neuropathy Diseases 0.000 claims description 2
- 230000035479 physiological effects, processes and functions Effects 0.000 claims description 2
- 229940079593 drug Drugs 0.000 claims 4
- 125000003275 alpha amino acid group Chemical group 0.000 claims 1
- 239000002552 dosage form Substances 0.000 claims 1
- 230000003449 preventive effect Effects 0.000 claims 1
- 208000017667 Chronic Disease Diseases 0.000 abstract description 7
- 210000000987 immune system Anatomy 0.000 abstract description 4
- 210000003169 central nervous system Anatomy 0.000 abstract description 3
- 102000004127 Cytokines Human genes 0.000 description 19
- 108090000695 Cytokines Proteins 0.000 description 19
- 241001494479 Pecora Species 0.000 description 18
- 210000004027 cell Anatomy 0.000 description 17
- 210000003022 colostrum Anatomy 0.000 description 16
- 235000021277 colostrum Nutrition 0.000 description 16
- 230000000694 effects Effects 0.000 description 14
- 108010047620 Phytohemagglutinins Proteins 0.000 description 13
- 201000010099 disease Diseases 0.000 description 13
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 13
- 230000001885 phytohemagglutinin Effects 0.000 description 13
- 102000014150 Interferons Human genes 0.000 description 12
- 108010050904 Interferons Proteins 0.000 description 12
- 229940079322 interferon Drugs 0.000 description 12
- 210000004698 lymphocyte Anatomy 0.000 description 12
- 238000000034 method Methods 0.000 description 12
- 108010074328 Interferon-gamma Proteins 0.000 description 11
- 241001465754 Metazoa Species 0.000 description 11
- 102100040247 Tumor necrosis factor Human genes 0.000 description 10
- 210000004369 blood Anatomy 0.000 description 10
- 239000008280 blood Substances 0.000 description 10
- 239000002158 endotoxin Substances 0.000 description 10
- 229920006008 lipopolysaccharide Polymers 0.000 description 10
- 239000000203 mixture Substances 0.000 description 10
- 108090000765 processed proteins & peptides Proteins 0.000 description 10
- 102100037850 Interferon gamma Human genes 0.000 description 9
- 238000012360 testing method Methods 0.000 description 9
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 description 7
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 7
- 150000001413 amino acids Chemical class 0.000 description 7
- 239000000411 inducer Substances 0.000 description 7
- 230000001939 inductive effect Effects 0.000 description 7
- 210000004877 mucosa Anatomy 0.000 description 7
- 229920001184 polypeptide Polymers 0.000 description 7
- 102000004196 processed proteins & peptides Human genes 0.000 description 7
- 102000009027 Albumins Human genes 0.000 description 6
- 108010088751 Albumins Proteins 0.000 description 6
- 206010003402 Arthropod sting Diseases 0.000 description 6
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 6
- 230000003203 everyday effect Effects 0.000 description 6
- 235000013373 food additive Nutrition 0.000 description 6
- 239000002778 food additive Substances 0.000 description 6
- 102000018358 immunoglobulin Human genes 0.000 description 6
- 239000000047 product Substances 0.000 description 6
- 108060003951 Immunoglobulin Proteins 0.000 description 5
- 241000124008 Mammalia Species 0.000 description 5
- 241000699670 Mus sp. Species 0.000 description 5
- 235000001014 amino acid Nutrition 0.000 description 5
- 229940024606 amino acid Drugs 0.000 description 5
- 238000005516 engineering process Methods 0.000 description 5
- 210000004700 fetal blood Anatomy 0.000 description 5
- 208000026278 immune system disease Diseases 0.000 description 5
- 230000036039 immunity Effects 0.000 description 5
- 210000000214 mouth Anatomy 0.000 description 5
- 230000000638 stimulation Effects 0.000 description 5
- 208000036142 Viral infection Diseases 0.000 description 4
- 230000004071 biological effect Effects 0.000 description 4
- 238000004440 column chromatography Methods 0.000 description 4
- 239000001963 growth medium Substances 0.000 description 4
- 208000015181 infectious disease Diseases 0.000 description 4
- 230000006996 mental state Effects 0.000 description 4
- 108090000623 proteins and genes Proteins 0.000 description 4
- 238000012207 quantitative assay Methods 0.000 description 4
- 239000003381 stabilizer Substances 0.000 description 4
- 239000003826 tablet Substances 0.000 description 4
- 230000001225 therapeutic effect Effects 0.000 description 4
- 238000002560 therapeutic procedure Methods 0.000 description 4
- RTKIYNMVFMVABJ-UHFFFAOYSA-L thimerosal Chemical compound [Na+].CC[Hg]SC1=CC=CC=C1C([O-])=O RTKIYNMVFMVABJ-UHFFFAOYSA-L 0.000 description 4
- 230000009385 viral infection Effects 0.000 description 4
- 241000283707 Capra Species 0.000 description 3
- 241000283074 Equus asinus Species 0.000 description 3
- 229920005654 Sephadex Polymers 0.000 description 3
- 239000012507 Sephadex™ Substances 0.000 description 3
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 3
- 239000004141 Sodium laurylsulphate Substances 0.000 description 3
- 210000000481 breast Anatomy 0.000 description 3
- 238000002512 chemotherapy Methods 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 230000018109 developmental process Effects 0.000 description 3
- 230000029087 digestion Effects 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 230000000527 lymphocytic effect Effects 0.000 description 3
- 210000002540 macrophage Anatomy 0.000 description 3
- 210000005087 mononuclear cell Anatomy 0.000 description 3
- 108010005636 polypeptide C Proteins 0.000 description 3
- 235000018102 proteins Nutrition 0.000 description 3
- 102000004169 proteins and genes Human genes 0.000 description 3
- 230000005855 radiation Effects 0.000 description 3
- 230000002441 reversible effect Effects 0.000 description 3
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 3
- 230000002269 spontaneous effect Effects 0.000 description 3
- 208000014644 Brain disease Diseases 0.000 description 2
- 241000282836 Camelus dromedarius Species 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- 108090000317 Chymotrypsin Proteins 0.000 description 2
- 208000020401 Depressive disease Diseases 0.000 description 2
- 238000002965 ELISA Methods 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 206010061598 Immunodeficiency Diseases 0.000 description 2
- 208000029462 Immunodeficiency disease Diseases 0.000 description 2
- 108090000723 Insulin-Like Growth Factor I Proteins 0.000 description 2
- 102000008070 Interferon-gamma Human genes 0.000 description 2
- 108090001005 Interleukin-6 Proteins 0.000 description 2
- 102000015696 Interleukins Human genes 0.000 description 2
- 108010063738 Interleukins Proteins 0.000 description 2
- 239000012980 RPMI-1640 medium Substances 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 102000013275 Somatomedins Human genes 0.000 description 2
- 241000700605 Viruses Species 0.000 description 2
- 230000003213 activating effect Effects 0.000 description 2
- 239000003708 ampul Substances 0.000 description 2
- 239000002269 analeptic agent Substances 0.000 description 2
- 230000003555 analeptic effect Effects 0.000 description 2
- 230000000844 anti-bacterial effect Effects 0.000 description 2
- 239000005018 casein Substances 0.000 description 2
- BECPQYXYKAMYBN-UHFFFAOYSA-N casein, tech. Chemical compound NCCCCC(C(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(CC(C)C)N=C(O)C(CCC(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(C(C)O)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(COP(O)(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(N)CC1=CC=CC=C1 BECPQYXYKAMYBN-UHFFFAOYSA-N 0.000 description 2
- 235000021240 caseins Nutrition 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 230000000295 complement effect Effects 0.000 description 2
- 230000003412 degenerative effect Effects 0.000 description 2
- 238000010612 desalination reaction Methods 0.000 description 2
- 238000009792 diffusion process Methods 0.000 description 2
- 239000000539 dimer Substances 0.000 description 2
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 2
- 238000001962 electrophoresis Methods 0.000 description 2
- 210000003725 endotheliocyte Anatomy 0.000 description 2
- 235000013305 food Nutrition 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 229940044627 gamma-interferon Drugs 0.000 description 2
- 239000000499 gel Substances 0.000 description 2
- 239000003292 glue Substances 0.000 description 2
- 235000020256 human milk Nutrition 0.000 description 2
- 210000004251 human milk Anatomy 0.000 description 2
- 230000007813 immunodeficiency Effects 0.000 description 2
- 230000003308 immunostimulating effect Effects 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- 230000006698 induction Effects 0.000 description 2
- 238000010255 intramuscular injection Methods 0.000 description 2
- 238000010253 intravenous injection Methods 0.000 description 2
- 230000006651 lactation Effects 0.000 description 2
- 238000009318 large scale farming Methods 0.000 description 2
- 230000002045 lasting effect Effects 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- 239000007937 lozenge Substances 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 230000035800 maturation Effects 0.000 description 2
- 235000012054 meals Nutrition 0.000 description 2
- 239000013642 negative control Substances 0.000 description 2
- 210000000056 organ Anatomy 0.000 description 2
- 239000002953 phosphate buffered saline Substances 0.000 description 2
- 239000011505 plaster Substances 0.000 description 2
- 239000002994 raw material Substances 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 210000000130 stem cell Anatomy 0.000 description 2
- 230000001954 sterilising effect Effects 0.000 description 2
- 238000004659 sterilization and disinfection Methods 0.000 description 2
- 230000004936 stimulating effect Effects 0.000 description 2
- 238000010254 subcutaneous injection Methods 0.000 description 2
- 229940124597 therapeutic agent Drugs 0.000 description 2
- 229940033663 thimerosal Drugs 0.000 description 2
- 239000013638 trimer Substances 0.000 description 2
- 229940035658 visco-gel Drugs 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 description 1
- WFIYPADYPQQLNN-UHFFFAOYSA-N 2-[2-(4-bromopyrazol-1-yl)ethyl]isoindole-1,3-dione Chemical compound C1=C(Br)C=NN1CCN1C(=O)C2=CC=CC=C2C1=O WFIYPADYPQQLNN-UHFFFAOYSA-N 0.000 description 1
- 208000029483 Acquired immunodeficiency Diseases 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 206010003974 Bacillary infections Diseases 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 206010006187 Breast cancer Diseases 0.000 description 1
- 208000026310 Breast neoplasm Diseases 0.000 description 1
- 206010006895 Cachexia Diseases 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- 208000013017 Child Nutrition disease Diseases 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- GUBGYTABKSRVRQ-WFVLMXAXSA-N DEAE-cellulose Chemical compound OC1C(O)C(O)C(CO)O[C@H]1O[C@@H]1C(CO)OC(O)C(O)C1O GUBGYTABKSRVRQ-WFVLMXAXSA-N 0.000 description 1
- 229920001917 Ficoll Polymers 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 102000008100 Human Serum Albumin Human genes 0.000 description 1
- 108091006905 Human Serum Albumin Proteins 0.000 description 1
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 1
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 1
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 206010027336 Menstruation delayed Diseases 0.000 description 1
- 241001529936 Murinae Species 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 206010029333 Neurosis Diseases 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 208000006268 Sarcoma 180 Diseases 0.000 description 1
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 1
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 1
- 239000004473 Threonine Substances 0.000 description 1
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 description 1
- 206010052428 Wound Diseases 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 230000004308 accommodation Effects 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000011543 agarose gel Substances 0.000 description 1
- 235000004279 alanine Nutrition 0.000 description 1
- 125000000539 amino acid group Chemical group 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 230000008485 antagonism Effects 0.000 description 1
- 230000002421 anti-septic effect Effects 0.000 description 1
- 230000000840 anti-viral effect Effects 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 235000003704 aspartic acid Nutrition 0.000 description 1
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 239000003124 biologic agent Substances 0.000 description 1
- 238000010170 biological method Methods 0.000 description 1
- 210000001124 body fluid Anatomy 0.000 description 1
- 239000010839 body fluid Substances 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 201000008275 breast carcinoma Diseases 0.000 description 1
- 229940046011 buccal tablet Drugs 0.000 description 1
- 239000006189 buccal tablet Substances 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 229910002092 carbon dioxide Inorganic materials 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 229940112822 chewing gum Drugs 0.000 description 1
- 235000015218 chewing gum Nutrition 0.000 description 1
- 230000035606 childbirth Effects 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 229960002376 chymotrypsin Drugs 0.000 description 1
- 238000010668 complexation reaction Methods 0.000 description 1
- 235000009508 confectionery Nutrition 0.000 description 1
- 239000012531 culture fluid Substances 0.000 description 1
- 235000018417 cysteine Nutrition 0.000 description 1
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 210000000981 epithelium Anatomy 0.000 description 1
- 210000003238 esophagus Anatomy 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 238000009313 farming Methods 0.000 description 1
- 239000012997 ficoll-paque Substances 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- -1 gelling Polymers 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- 210000003714 granulocyte Anatomy 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 1
- 208000007475 hemolytic anemia Diseases 0.000 description 1
- 230000002607 hemopoietic effect Effects 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 150000002430 hydrocarbons Chemical class 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 239000002955 immunomodulating agent Substances 0.000 description 1
- 230000002584 immunomodulator Effects 0.000 description 1
- 229940121354 immunomodulator Drugs 0.000 description 1
- 230000007365 immunoregulation Effects 0.000 description 1
- 230000004957 immunoregulator effect Effects 0.000 description 1
- 230000001976 improved effect Effects 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 230000002458 infectious effect Effects 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 229910017053 inorganic salt Inorganic materials 0.000 description 1
- 238000004255 ion exchange chromatography Methods 0.000 description 1
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 1
- 229960000310 isoleucine Drugs 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 206010025482 malaise Diseases 0.000 description 1
- 210000005075 mammary gland Anatomy 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- 235000013336 milk Nutrition 0.000 description 1
- 239000008267 milk Substances 0.000 description 1
- 210000004080 milk Anatomy 0.000 description 1
- 210000002161 motor neuron Anatomy 0.000 description 1
- 229920001206 natural gum Polymers 0.000 description 1
- 229930014626 natural product Natural products 0.000 description 1
- 230000002981 neuropathic effect Effects 0.000 description 1
- 208000015238 neurotic disease Diseases 0.000 description 1
- 210000000440 neutrophil Anatomy 0.000 description 1
- 239000001814 pectin Substances 0.000 description 1
- 235000010987 pectin Nutrition 0.000 description 1
- 229920001277 pectin Polymers 0.000 description 1
- 238000010647 peptide synthesis reaction Methods 0.000 description 1
- 238000011056 performance test Methods 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 210000004303 peritoneum Anatomy 0.000 description 1
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 1
- 238000002264 polyacrylamide gel electrophoresis Methods 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 238000001959 radiotherapy Methods 0.000 description 1
- 238000010188 recombinant method Methods 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 210000000664 rectum Anatomy 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 210000002345 respiratory system Anatomy 0.000 description 1
- 210000003296 saliva Anatomy 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 230000035807 sensation Effects 0.000 description 1
- ZEYOIOAKZLALAP-UHFFFAOYSA-M sodium amidotrizoate Chemical compound [Na+].CC(=O)NC1=C(I)C(NC(C)=O)=C(I)C(C([O-])=O)=C1I ZEYOIOAKZLALAP-UHFFFAOYSA-M 0.000 description 1
- 229950005811 sodium amidotrizoate Drugs 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 210000002536 stromal cell Anatomy 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 230000009747 swallowing Effects 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 231100000820 toxicity test Toxicity 0.000 description 1
- 238000009602 toxicology test Methods 0.000 description 1
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 1
- 239000004474 valine Substances 0.000 description 1
- 239000011782 vitamin Substances 0.000 description 1
- 229930003231 vitamin Natural products 0.000 description 1
- 235000013343 vitamin Nutrition 0.000 description 1
- 229940088594 vitamin Drugs 0.000 description 1
- 150000003722 vitamin derivatives Chemical class 0.000 description 1
- 230000003442 weekly effect Effects 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/17—Amino acids, peptides or proteins
- A23L33/18—Peptides; Protein hydrolysates
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/17—Amino acids, peptides or proteins
- A23L33/19—Dairy proteins
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/40—Complete food formulations for specific consumer groups or specific purposes, e.g. infant formula
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/22—Anxiolytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/30—Drugs for disorders of the nervous system for treating abuse or dependence
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/02—Nutrients, e.g. vitamins, minerals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2002/00—Food compositions, function of food ingredients or processes for food or foodstuffs
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2200/00—Function of food ingredients
- A23V2200/30—Foods, ingredients or supplements having a functional effect on health
- A23V2200/324—Foods, ingredients or supplements having a functional effect on health having an effect on the immune system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
Abstract
本发明涉及初乳肽的制药应用。具体而言,本发明涉及初乳肽及其有效片段九肽制备用于治疗慢性中枢神经系统和免疫系统疾病的药物的应用。
Description
本发明涉及初乳肽(colostrinin)及其作为药物的用途。
初乳是由雌性哺乳动物乳房在分娩后最初数天内产出的黄色粘稠液体。分娩4至5天后它将被成熟母乳替代。与成熟母乳相比,初乳含糖较低。然而,初乳中却含有丰富的脂类、蛋白质、无机盐、维生素和免疫球蛋白。并且它还含有多种飘浮细胞,例如粒细胞、基质细胞、嗜中性白细胞、单核细胞、巨噬细胞、淋巴细胞,以及生长因子、激素和细胞因子。
已从哺乳动物初乳中分离并定性了多种因子。1974年,Janusz等人(FEBS Lett.,49,276-279)从绵羊初乳中分离出一种高脯氨酸含量的多肽(PRP)。该参考文献的内容在此引入作为参考。业已发现,除绵羊以外的哺乳动物都以PRP的类似物作为初乳的组分。PRP也因此称作初乳肽,并且被暂定成一类新的细胞因子。
Janusz等人在“高脯氨酸含量的多肽(PRP)一绵羊初乳中的一种免疫调制肽”(Archivum Immunologiae et Therapiae Experimentalis,1993,41,275-279)中指出,绵羊初乳的PRP对小鼠具有亲免活性。然而,该文献却没有报导PRP对其他动物有任何治疗作用。事实上应承认,从一种对小鼠有治疗作用的组合物并不能预见到它也对其他任何动物有治疗作用。
本申请人发现,初乳肽具有许多前所未知的治疗功效。具体而言,我们发现初乳肽可显现出亲免作用和精神病治疗作用。
作为本发明的一个方面,本申请人提供了用作药物的初乳肽。所述初乳肽可作为药物用于非啮齿动物;我们还发现,所述初乳肽特别适合作为治疗人类的药物。
另一方面,本发明提供了初乳肽在制备治疗中枢神经系统疾病或免疫系统疾病用药物中的应用。
在本发明的一个优选实施例中,所述初乳肽被用来治疗中枢神经系统的疾病,尤其是中枢神经系统的慢性疾病。可以用初乳肽治疗的中枢神经系统病包括神经病和精神病。
适合用初乳肽治疗的神经病的例子包括:痴呆,诱发痴呆的疾病,例如神经变性疾病。神经变性疾病包括,例如老年性痴呆和运动神经元病;帕金森氏病是一个可用初乳肽治疗的运动神经元疾病的实例。现已发现,初乳肽在治疗称作早老性痴呆的神经变性疾病中特别有效。
适合用初乳肽治疗的精神病的例子包括:精神病和神经官能症。例如,可用初乳肽治疗情绪紊乱,特别是治疗处于抑郁状态的精神病患者的情绪紊乱—已发现初乳肽帮助患者改善感觉安宁和心境安定。初乳肽还可以在药物癖嗜者、解毒期以后以及兴奋剂依赖性人群中用作辅助性戒除治疗剂。
在本发明的另一个优选实施例中,所述初乳肽被用于治疗免疫系统的疾病,尤其是慢性免疫系统疾病。因此我们发现,可在需要免疫调节的疾病治疗中采用所述初乳肽。特别是,初乳肽适合治疗包括人类在内的非啮齿动物的上述疾病。初乳肽在治疗许多基于免疫和感染的疾病中十分有效。例如,用初乳肽治疗与细菌病原和病毒病原有关的慢性疾病,还可以治疗继发的,例如肿瘤化疗和放疗继发的获得性免疫缺损。本发明特别适合治疗需要非特异性免疫刺激和免疫校正的细菌性和病毒性慢性传染病。
通常,慢性病是一种持续时间较长的疾病,常常至少一周,更常见至少一个月,并且经常是至少3个月或至少6个月。
本发明的特征之一是用初乳肽改善新生儿免疫系统的发育。本发明的另一特征在于用初乳肽校正儿童的免疫缺乏。所述初乳肽的这些用途特别适合未曾获得初乳的婴儿或儿童。而这种情况发生在,例如,出生后没有母乳喂养的婴儿和儿童中;在给这些婴儿和儿童的人工食物中不含有初乳肽。
本发明的另一方面中,我们提供了初乳肽作为食品强化剂的用途。所述初乳肽特别适合用作婴儿和幼童的食品强化剂,以校正其免疫系统发育中的缺乏。正如上文所述,这种缺乏发生在出生后未母乳喂养的婴儿和儿童中。所述初乳肽也可以作为接受化疗或患有恶病质或因慢性病而体重减轻的成人的食品强化剂。作为本发明的一个方面,我们提供了一种含有与生理可接受载体合用的口服可摄取初乳肽结合物的食品强化剂。该食品强化剂是液体或固体的形式;也适于将其以片剂形式供给。
本发明中可预防性给予所述初乳肽,以便有助于预防中枢神经系统疾病和免疫系统疾病的发展。
本发明上述初乳肽可以是绵羊初乳肽,或者是非绵羊产的初乳肽。非绵羊产的初乳肽可以从,例如人、母牛、马、山羊、猪、牦牛、美洲驼和驴的初乳中获得。初乳肽通常存在于上述动物分娩后1至4天后的初乳中。
此处的术语“初乳肽”是指一种从哺乳动物初乳中获得的天然形式的多肽。有时初乳肽也称作“colostrinine”,并且具有下列性质:
(i)分子量在16,000至26,000道尔顿之间;
(ii)它是亚单位的二聚体或三聚体,各亚单位的分子量是5,000至10,000道尔顿,优选6,000道尔顿;
(iii)它含有脯氨酸,并且脯氨酸的含量高于其他任何一种氨基酸的量。
我们发现,所述初乳肽以及组成它的亚单位都是非极性的。
在SDS(十二烷基硫酸钠)存在下采用电泳法可对所述初乳肽的分子量进行测定;这种技术也可显示出存在的二聚体和三聚体。还原或非还原条件的电泳皆表明,亚单位之间的键是非共价键。通过常规的氨基酸分析技术可以确定存在的脯氨酸。非极性色谱可能够证实初乳肽的非极性。
本发明所用初乳肽可以是绵羊初乳肽或非绵羊初乳肽。绵羊初乳肽的分子量约为18,000道尔顿,并且由三个非共价键合亚单位组成,每个亚单位的分子量分别是约6,000道尔顿,其中含有22%重量的脯氨酸。每个亚单位的氨基酸组成由数量如下的残基构成:赖氨酸-2、组氨酸-1、精氨酸-0、天门冬氨酸-2、苏氨酸-4、丝氨酸-3、谷氨酸-6、脯氨酸-11、甘氨酸-2、丙氨酸-0、缬氨酸-5、蛋氨酸-2、异亮氨酸-2、亮氨酸-6、酪氨酸-1、苯丙氨酸-3和半胱氨酸-0。
如上所述,天然形式的初乳肽来源于哺乳动物的初乳。通过除去初乳中的脂类和多数蛋白质可以获取哺乳动物初乳的初乳肽。广义上,初乳肽是从例如大型畜牧动物的初乳中通过柱色谱技术和其他生物技术获得,或者通过基因工程技术来制得。
具体而言,可以通过下列步骤从哺乳动物初乳中分离出初乳肽:
(i)脱脂,例如通过离心法;
(ii)去除蛋白质(例如酪蛋白),例如通过降低pH;
(iii)分离出与免疫球蛋白键合的初乳肽,例如通过:
(a)对脱脂和除蛋白后的乳清进行离子交换色谱;和
(b)用磷酸盐缓冲盐水洗脱,并收集含有与免疫球蛋白,例如绵羊的IgG2键合的初乳肽的馏分;
(iv)从免疫球蛋白上分离初乳肽,例如采用筛分色谱法;和
(v)提纯初乳肽,优选通过:
(a)将分子量低于30,000道尔顿的部分进行脱盐;和
(b)为免疫球蛋白引入抗体,由此除去此类蛋白质,得到终产物。
尽管上述定义是指天然的哺乳动物初乳肽,但此处的术语“初乳肽”也包括其生物活性基本相同的类似物和片断,以及通过DNA重组技术生产的哺乳动物初乳肽、其类似物或片断。此处的初乳肽还包括通过多肽合成技术制备的、组成与天然初乳肽基本相同的生物活性多肽。
本发明另一方面提供了一种用初乳肽治疗中枢神经系统疾病或免疫系统疾病的方法。上文已对适合用本发明所述方法治疗的疾病作了描述。在本发明一个优选实施例中,患者接受初乳肽的第一阶段给药,该第一阶段中每天给予约1至2个治疗单位,随后是没有初乳肽给药的第二阶段。所述第一阶段优选是约2至4周,更优选约3周;并且,第二阶段优选约2至5周,更优选约4周。优选至少重复一次这种治疗循环,并且更优选重复不止一次。
本发明方法中所用的治疗单位优选25至1,000微克,更优选50至100微克的初乳肽。
可以将初乳肽制成适当的形式来给药。例如,制成口服、直肠或非肠道给药的形式。具体而言,可将初乳肽配制成注射剂给药,或者优选配制成适合通过口腔/鼻咽腔粘膜、食道或其他粘膜表面吸收的形式给药。所述口服制剂可以是适于吞咽的形式;或优选溶于唾液的形式,这种制剂是在口腔/鼻咽腔粘膜内吸收。所述口服制剂也可以是口服给药的片剂、糖锭(即适合留在口腔内含服的甜片)、可咀嚼成口胶的粘性凝胶。还可将所述初乳肽配制成胶用粘性硬膏或贴剂。所述初乳肽还可以是涂敷在生殖泌尿器官粘膜上的制剂。
当然,尽管能够以完整初乳的形式给予所述初乳肽,但这并不可取,因为完整的初乳具有不适的味道并且难以储存。
本发明所用初乳肽可以来源于任何哺乳动物,例如取自人类或动物,例如母牛、马、山羊、猪、牦牛、绵羊、美洲驼或驴、骆驼等。
对绵羊初乳肽和人初乳肽进行试验。绵羊的初乳肽以ColostrininTM的商标出售。
在动物试验中发现,初乳肽的特征是其体内外亲免作用,这种亲免作用是基于对胸腺细胞向活性T细胞分化和成熟的发展的调节性质,基于对免疫反应的刺激或抑制作用,并且基于对胸腺细胞上多种表面标记的表达的诱导作用。在对小鼠腹膜内给药中,初乳肽可抑制NZB系小鼠溶血性贫血的发展,也抑制小鼠肉瘤180的生长,并且对于受到γ射线照射的小鼠,初乳肽可以保护该动物对抗放射病。小鼠的毒理学试验表明,口服和非肠道给药后毒性极低,这是由于LD50高于1.25g/kg体重。初乳肽还表现出对人和试验动物中免疫活性细胞的生长、成熟和分化的刺激能力。在人外周血液的淋巴细胞培养物(包括从脐带血中分离出的淋巴细胞的培养物)中,初乳肽的特征在于:它可刺激细胞因子,特别是γ-干扰素(IFN-γ)、肿瘤坏死因子(TNF-α)、白介素类(例如IL-6和IL-10)以及多种生长因子的产生。通过已知方法可以定量测定所生产的细胞因子。
在自然状况下,分娩后1至4天内,人的初乳和所有哺乳动物,尤其是大型畜牧动物(例如母牛、马、山羊、猪、牦牛、绵羊、美洲驼或驴、骆驼等)的初乳中都存在具有该生化活性的绵羊初乳肽类似物。初乳肽在新生动物吸吮和吞咽母体初乳的过程中进入到体内。由于初乳肽分子量较低,初乳肽可以在口腔/鼻咽腔粘膜上通过细胞受体起作用,甚至进行简单扩散(ordinary diffusion)。研究表明,由于消化道上段的粘膜和上皮含有某些免疫调制剂的受体,所述初乳肽可以以片剂和舌下含片、吞咽用片剂和胶囊、粘性凝胶形式以及与树胶固定在一起的粘性硬膏形式来给药。也可以将初乳肽涂敷在生殖泌尿器官的粘膜上。
以弄清初乳肽所诱导的生化活性为目的的科学试验还揭示了,来源于产后1至7天妇女的人类初乳具有类似生物活性。人体原料中初乳肽的分离方法类似于从畜牧动物的初乳,尤其是绵羊初乳中获取初乳肽的方法。由产后1至7天妇女乳腺分泌的初乳含有多肽类的初乳肽,它的量取决于泌乳作用,并且在2至3天内最佳,此时1升初乳中可检测出300mg初乳肽。这样的人初乳肽产量可见于绵羊初乳中。现已证明,人初乳肽具有许多与例如绵羊产类似物相似的生物性质。来源于人初乳的初乳肽可刺激初乳所含淋巴细胞以及脐血淋巴细胞分泌细胞因子,所述细胞因子主要包括干扰素(IFN-γ)、肿瘤坏死因子TNF-α、白介素类(IL-10和IL-6)或其它细胞因子。这些细胞因子参与体液和细胞的免疫反应。
采用公开在波兰专利(PL 170592B1)和欧洲专利EP-B-0609225中的性能试验免疫学方法,可对人和动物来源的初乳肽的生物活性进行测定。
在对人类志愿者的研究中发现,用至少含有25μg初乳肽的含片以每天至少一片的剂量给药约3周后,没有观察到任何副作用;另一方面,却形成一种对诱导IFN-γ以及部分肿瘤坏死因子TNF-α的低反应状态。在停止初乳肽给药后,这种低反应性状态将恢复正常。这些反应的结果是Th1和Th2淋巴细胞和辅助细胞产生细胞因子。
临床试验还表明,初乳肽具有免疫调节作用以及对中枢神经系统的作用,它可以预防性和治疗性地应用于下列疾病,例如,用于预防早老性痴呆的出现和进行,并缓解这种疾病;也可应用于一些其它起因的老年性痴呆,并可治疗与免疫和感染有关的慢性疾病。
可用具有下列组成和氨基酸序列的、缩写为NP的九肽取代初乳肽:Val-Glu-Ser-Tyr-Val-Pro-Leu-Phe-Pro。通过糜蛋白酶的消化作用和柱色谱的分离,可从初乳肽中获取NP,或者通过化学合成法来制得NP。NP是初乳肽有效片段的一个例子。现已发现,NP具有与初乳肽相似的生物作用,特别是,它适合治疗上述慢性免疫疾病和中枢神经系统疾病(尤其是早老性痴呆)。可以用NP治疗上述任何一种疾病。也可以将它应用于食品强化剂中。可以按照与初乳肽相同的方法来配制它。NP适合治疗哺乳动物,尤其是人类。
为了更全面地理解本发明,可以参考下列仅作说明作用的实施例。实施例1
分子量18,000道尔顿的绵羊初乳肽是由三个非共价连接的亚单位构成,亚单位的分子量为6000道尔顿,各亚单位具有下列氨基酸组成:
| 氨基酸 | 每个亚单位中的残基数量 |
| 赖氨酸 | 2 |
| 组氨酸 | 1 |
| 精氨酸 | 0 |
| 天门冬氨酸 | 2 |
| 苏氨酸 | 4 |
| 丝氨酸 | 3 |
| 谷氨酸 | 6 |
| 脯氨酸 | 11 |
| 甘氨酸 | 2 |
| 丙氨酸 | 0 |
| 缬氨酸 | 5 |
| 蛋氨酸 | 2 |
| 异亮氨酸 | 6 |
| 酪氨酸 | 1 |
| 苯丙氨酸 | 3 |
| 半胱氨酸 | 0 |
所用初乳肽来源于在绵羊分娩至多24小时后泌乳开始后的绵羊初乳。将原料在35000×g离心,以便除去脂肪及部分酪蛋白。将所得部分的1g置于DEAE-纤维素柱中,从而分离出与免疫球蛋白IgG2络合的多肽初乳肽,利用葡聚糖凝胶G-100柱色谱法以及用葡聚糖凝胶G-75再次进行的色谱,可从柱中洗脱出与IgG2分离的初乳肽。随后,将一部分多肽通过结合有绵羊IgG2抗体的琼脂糖凝胶柱,以除去痕量的IgG2杂质。所得制备物通过葡聚糖凝胶G-25的方式脱盐并冷冻干燥,此后将其储存在+4℃或-20℃下。
所得初乳肽的商标名被命名为ColostrininTM。
在有SDS存在的聚丙烯酰胺凝胶电泳中,在与分子量5 800道尔顿相对应处可以观察到一个强带,同时还出现两个弱带,它们分别与分子量12 400道尔顿和18 200道尔顿相对应。实施例II
从实施例1所述初乳肽中可以得到九肽NP,NP的组成和氨基酸序列为Val-Glu-Ser-Tyr-Val-Pro-Leu-Phe-Pro。
通过10个活性单位的蛋白水解酶糜蛋白酶在30℃的温度下对50mg初乳肽进行20小时的消化。对消化产物的分离应通过至少一个循环的葡聚糖凝胶G-10柱色谱。冻干所得制备物,随后储存在+4℃或-20℃的温度下。通过测定N-末端氨基酸对九肽进行分离。实施例III
吸吮片形式的剂量单位具有下列组成:活性成分: 实施例1所得的Colostrinin多肽 0.0001g稳定剂: 白蛋白,无杂质,主要I.P.S 0.000135g润滑剂/粘合剂:硬脂酸镁 0.003g载体: 甘露糖醇 0.1g(0.1497g)
将上述组分悬浮在0.0001M NaCl中。吸吮片主要用于治疗早期和晚期痴呆症(包括早老性痴呆)以及不同时期的老年性痴呆;还可以治疗慢性细菌性及病毒性感染、所需的非特异性免疫刺激和免疫校正以及由多种试剂诱发的获得性免疫缺乏。此外,也可用它治疗情绪紊乱,特别是治疗不同抑郁状态的精神病患者,从而改善他们的全身安全感和心境稳定性;初乳肽还可以在药物癖嗜者、解毒期以后以及兴奋剂依赖性人群中用作辅助性戒除治疗剂。ColostrininTM也可以作为人工食品来校正新生儿和幼童的营养缺乏。实施例IV
制备具有下列组成的粘膜涂敷用凝胶形式:活性成分: 实施例1所得ColostrininTM多肽稳定剂: 白蛋白胶凝载体: Orabase-Plain,它含有果胶、胶凝、羧甲基纤维素钠
和碳氢化合物胶
每1ml凝胶载体使用0.0003g多肽ColostrininTM和0.0015g白蛋白。如此配制的剂量单位主要用于口腔和上呼吸道细菌性及病毒性感染的循环治疗。实施例V
肌肉内、皮下或静脉内注射形式的制剂。活性成分:实施例1所得ColostrininTM多肽稳定剂: 人白蛋白,无杂质胶凝载体:灭菌的无热原水
每1ml安瓿中使用0.0003g ColostrininTM多肽、0.0015g白蛋白、作为抗菌剂的0.001%硫柳汞(即乙汞硫代水杨酸钠盐)。这种剂量单位主要用于细菌性和病毒性感染的循环治疗。实施例VI
肌肉内、皮下或静脉内注射形式的制剂。活性成分:实施例II所得NP稳定剂: 白蛋白,无杂质胶凝载体:灭菌的无热原水
每1ml安瓿中使用0.0003gNP、0.0015g白蛋白、作为抗菌剂的0.001%硫柳汞(即乙汞硫代水杨酸钠盐)。这种剂量单位主要用于细菌性和病毒性感染的循环治疗。实施例VII
按照下列方法从接受实施例III所述药物形式循环治疗的健康和患病志愿者中采集血液,分析血中多肽ColostrininTM对体外细胞因子的诱导作用。
将不含防腐剂但每1ml含有10个单位肝素的全血以1∶10的配比稀释在RPMI1640培养基中。在37℃和含有5%二氧化碳的条件下于相同培养基中孵育20小时,孵育所用培养基不含有诱导物(阴性对照),或者含有1至100μg/ml多肽ColostrininTM,或含有2μg/ml血的植物凝集素(PHA)和2μg/ml血的脂多糖(LPS)。含有PHA和LPS的混合物的样品作为阳性对照物,原因在于它们可以刺激最高量的细胞因子。表1和2中列出了试验结果。结果表明,ColostrininTM在1至100μg/ml的浓度下以剂量依赖方式刺激细胞因子的产生。与阴性对照物(不含诱导物)比较,这些结果有统计学意义(p<0.0001)。早老性痴呆患者的IFN生产能力降低,并且TNF的也较小程度地降低。表1
绵羊ColostrininTM(系列A 1993)在健康志愿者或早老性痴呆患者的全血淋巴细胞培养物中的细胞因子诱导作用
| 供血者 | 诱导物 | 剂量(μg/lm) | 细胞因子(单位/ml±SD) | |
| IFN | TNF | |||
| ColostrininTM | 100 | 344±254 | 670±560 | |
| 健康志愿者 | ColostrininTM | 10 | 50±59 | 316±371 |
| PHA+LPS | 2+2 | 171±162 | 521±447 | |
| 空白对照 | - | 9±21 | 19±26 | |
| ColostrininTM | 100 | 21±14 | 249±187 | |
| 早老性痴呆 | ColostrininTM | 10 | 15±9 | 182±158 |
| 患者 | PHA+LPS | 2+2 | 117±76 | 397±252 |
| 空白对照 | - | 2±3 | 18±26 | |
健康志愿者组(22人)的年龄各不相同(年龄在20至64岁间)。早老性患者组(50人)年龄也不相同(年龄63±7.5岁)。尽管不含(无)诱导物的空白对照组之间的标准偏差(±SD)差异性较大,但ColostrininTM有统计学意义(p<0.001)。
表2绵羊ColostrininTM(A系列1993)在用健康志愿者和多种疾病患者全血
进行的试验中对干扰素(IFN)生产的刺激例供血者 诱导物 剂量(μg/ml) IFN的效价,其测定通过
-----------------------------(诊断) 抗病毒 ELISA IFN-γ
生物试验 pg/ml
(单位/ml)Z.B. ColostrininTM 100 300 2920健康 ColostrininTM 10 300 3402年轻士兵 ColostrininTM 1 100 1413
PHA+LPS 2+2 200 3308
空白对照 - <3 24C.D. ColostrininTM 100 600 3941健康 ColostrininTM 10 200 3778年轻士兵 ColostrininTM 1 100 2690
PHA+LPS 2+2 600 4631
空白对照 - 5 55M.J. ColostrininTM 100 40 400早老性 ColostrininTM 10 20 427痴呆患者 PHA+LPS 2+2 300 3757
空白对照 - 3 46S.E. ColostrininTM 100 6 29精神 ColostrininTM 10 6 29分裂症 PHA+LPS 2+2 30 243
空白对照 - 3 19F.W. ColostrininTM 100 70 523乳腺癌 ColostrininTM 10 50 307
PHA+LPS 2+2 600 2833
空白对照 - 40 150附注:对存在的IFN进行的生物试验可以测出不同类型干扰素的含量,而ELISA试验仅检测免疫活性IFN-γ的水平。实施例VIII
从Wroclaw的地区专业医院的妇产科获得脐带血。在产后4至6小时获取的脐带血的淋巴细胞中,ColostrininTM通过下列途径体外有效诱导细胞因子。
用每100ml含有5.7g Ficoll 400和9.0g泛影酸钠的Ficoll-Paque梯度物分离淋巴细胞。以每1ml培养基2×106个淋巴细胞的密度将分离的淋巴细胞悬浮在RPMI-1640培养基中。向该淋巴细胞悬浮液中加入浓度为1至20μg/ml的ColostrininTM或10μg/ml植物凝集素。将该培养物在37℃下孵育20小时。随后通过生物学方法对培养液中细胞因子的水平进行检测。表3中给出了一个典型实例。1至100μg/ml浓度的ColostrininTM所具有的细胞因子(IFN和TNF)刺激作用与传统IFN-γ诱导物—植物凝集素的相类似。
表3
ColostrininTM(A系列1996)在脐带血淋巴细胞培养物(CBL)
中的细胞因子诱导作用N 诱导物 剂量(μg/ml) 细胞因子(单位/ml±SD)
-----------------------------
IFN TFN32 ColostrininTM 20 89±79 59±4139 ColostrininTM 10 78±80 37±3517 ColostrininTM 1 38±66 16±1750 PHA 10 75±66 83±6950 空白对照 - 3±3 3±4N-被检测CBL样品数学生t-检验中,ColostrininTM的显著性差异几率(p)-IFN和TNF中所用的“无”是p<0.0001。
由于脐带血中富含未成熟干细胞,而这种细胞能够繁殖成造血细胞和多种免疫活性细胞,所以ColostrininTM极大地加快了干细胞的成熟。结果还表明,ColostrininTM可以有效治疗不同类型的免疫缺陷,也可以在例如外伤、感染、化疗和放疗后用于刺激造血系统。在生物医学研究中,具有类似作用的天然产物很罕见。实施例IX
对一组患有早期和中期早老性痴呆症的志愿者进行中枢神经系统疾病疗法的试验。所用剂量单位以吸吮片形式在两餐之间给药,该剂量单位含有0.00015实施例I和III所述的ColostrininTM。首先,每天使用一片并持续3周,随后中止治疗达2至4周,此后再次进行治疗并且每天服用2片且持续3周。发现ColostrininTM疗法可诱导一种低反应性或耐受的状态。这表明没有合成IFN及肿瘤坏死因子TNF-α的能力。可以用这种现象对活性剂的功效进行定量测定。
在中止上述药物的给药后,这种耐受状态也发生自发性逆转。ColostrininTM的这种暂时性耐受状态归因于由Th1和Th2淋巴细胞、辅助细胞所产生的细胞因子,所述辅助细胞例如是单核细胞、巨噬细胞、树状细胞、内皮细胞及其产物。其结果是,可在早老性痴呆患者中观察到人际关系的改善和心境高涨。
附图1图示了女性早老性痴呆患者(J.M)中的对于γ-干扰素(IFN-γ)诱导作用的低反应性状态部分耐受的出现以及自然消失,这些患者每隔一天服用100μg的ColostrininTM片剂并持续3周。随后将治疗中止3周(在暂定期间,对诱导物的耐受性恢复正常)。每周采集血样以用于检测ColostrininTM和空白对照(PHA-10μg/ml)的IFN-γ刺激作用。上文部分已描述了进行细胞因子诱导试验及其定量测定的方法。
被诱导IFN-γ水平的检测结果表明,低反应性早在服用ColostrininTM(每2天100μg/片)的第一周即出现并在治疗的第三周达到最高值。在中止治疗的3周内(即治疗开始后第6周内),对IFN-γ诱导作用的耐受状态发生自发性逆转。并且,该附图表示,“特别是”绵羊ColostrininTM(OvCal),这种低反应性在观察的第6周仍能够维持,而PHA低反应性却完全消失。实施例X
对一组患有早期早老性痴呆症的志愿者进行中枢神经系统疾病疗法的试验。所用剂量单位以吸吮片形式在两餐之间给药,该剂量单位含有0.00015实施例II所述NP。首先,每天使用一片并持续3周,随后中止治疗达3周,此后再次进行治疗并且每天服用2片且持续3周。发现NP疗法可诱导一种低反应性或耐受的状态。这表明没有合成IFN及肿瘤坏死因子TNF-α的能力。可以用这种现象对活性剂的功效进行定量测定。
在中止上述药物的给药后,这种耐受状态发生自发性逆转。NP的这种暂时性耐受状态归因于由Th1和Th2淋巴细胞、辅助细胞所产生的细胞因子,所述助细胞例如是单核细胞、巨噬细胞、树状细胞、内皮细胞及其产物。其结果是,可在早老性痴呆患者中观察到人际关系的改善和心境高涨。
Claims (12)
1.初乳肽在制备用于治疗慢性中枢神经系统疾病的药物中的应用。
2.权利要求1的应用,其中所述药物是用于治疗神经病和/或精神病的药物。
3.权利要求1的应用,其中所述药物是用于治疗痴呆和/或神经变性疾病的药物。
4.权利要求1的应用,其中所述药物是用于治疗早老性痴呆的药物。
5.权利要求1的应用,其中所述药物是用于治疗运动神经元疾病的药物。
6.权利要求1的应用,其中所述药物是用于治疗精神病和/或神经官能症的药物。
7.权利要求1的应用,其中所述药物是用于防止或抑制早老性痴呆发生的人用预防性药物。
8.权利要求1~7之任一项的应用,其中所述初乳肽为非绵羊初乳肽。
9.权利要求1~7之任一项的应用,其中所述药物为与生理学可接受的载体组合的口服剂型。
10.权利要求1~7之任一项的应用,其中所述初乳肽为分离的形式。
11.组成和氨基酸序列是Val-Glu-Ser-Tyr-Val-Pro-Leu-Phe-Pro的九肽在制备用于治疗慢性中枢神经系统疾病的药物中的应用。
12.权利要求11的应用,其中所述药物是用于治疗早老性痴呆的药物。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PL96316416A PL185442B1 (pl) | 1996-10-03 | 1996-10-03 | Środek farmaceutyczny o działaniu immunologicznym i psychotropowym, jego postać terapeutyczna oraz zastosowanie |
| PLP.316416 | 1996-10-03 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNA031466095A Division CN1535722A (zh) | 1996-10-03 | 1997-10-03 | 初乳肽及其用途 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN1238782A CN1238782A (zh) | 1999-12-15 |
| CN1131712C true CN1131712C (zh) | 2003-12-24 |
Family
ID=20068412
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNA031466095A Pending CN1535722A (zh) | 1996-10-03 | 1997-10-03 | 初乳肽及其用途 |
| CN97198535A Expired - Fee Related CN1131712C (zh) | 1996-10-03 | 1997-10-03 | 初乳肽及其用途 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNA031466095A Pending CN1535722A (zh) | 1996-10-03 | 1997-10-03 | 初乳肽及其用途 |
Country Status (18)
| Country | Link |
|---|---|
| US (2) | US6852700B1 (zh) |
| EP (1) | EP0932623A1 (zh) |
| JP (2) | JP2001501929A (zh) |
| KR (2) | KR100508764B1 (zh) |
| CN (2) | CN1535722A (zh) |
| AR (1) | AR013612A1 (zh) |
| AU (1) | AU4565197A (zh) |
| BR (1) | BR9712259A (zh) |
| CA (1) | CA2266859C (zh) |
| CZ (1) | CZ298215B6 (zh) |
| GB (1) | GB2333453B (zh) |
| HU (1) | HUP9904368A3 (zh) |
| IL (1) | IL129211A (zh) |
| PL (1) | PL185442B1 (zh) |
| RU (1) | RU2217152C2 (zh) |
| TR (1) | TR199901022T2 (zh) |
| WO (1) | WO1998014473A1 (zh) |
| ZA (1) | ZA978885B (zh) |
Families Citing this family (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| PL185442B1 (pl) | 1996-10-03 | 2003-05-30 | Georgiades Biotech Ltd | Środek farmaceutyczny o działaniu immunologicznym i psychotropowym, jego postać terapeutyczna oraz zastosowanie |
| EP1080111B1 (en) | 1998-05-27 | 2012-07-25 | Gemma Biotechnology Ltd. | The induction of antiobiotic peptides by lait (scd14) protein |
| AU777968B2 (en) * | 1998-06-10 | 2004-11-04 | Albert B. Crum | Prophylactic and therapeutic nutritional supplement for creation/maintenance of health-protective intestinal microflora and enhancement of the immune system |
| GB9813031D0 (en) * | 1998-06-16 | 1998-08-12 | Regen Biotech Limited | Dietary supplement |
| GB9912852D0 (en) * | 1999-06-02 | 1999-08-04 | Regen Therapeutics Plc | Peptides |
| EP1238058B1 (en) * | 1999-08-17 | 2007-10-03 | The University Of Texas System | Use of colostrinin, constituent peptides and analogs thereof to promote neural cell differentiation |
| US6903068B1 (en) * | 1999-08-17 | 2005-06-07 | Board Of Regents, The University Of Texas System | Use of colostrinin, constituent peptides thereof, and analogs thereof for inducing cytokines |
| AU7061700A (en) * | 1999-08-17 | 2001-03-13 | University Of Texas System, The | Use of colostrinin, constituent peptides thereof, and analogs thereof as oxidative stress regulators |
| US7119064B2 (en) * | 1999-08-17 | 2006-10-10 | Board Of Regents, The University Of Texas System | Use of colostrinin, constituent peptides thereof, and analogs thereof as modulators of intracellular signaling molecules |
| US6852685B1 (en) * | 1999-08-17 | 2005-02-08 | Board Of Regents, The University Of Texas System | Use of colostrinin, constituent peptides thereof, and analogs thereof to promote neuronal cell differentiation |
| EP1224217A4 (en) * | 1999-08-17 | 2006-05-24 | Univ Texas | USE OF COLOSTRININ, THOSE FORMING PEPTIDES, AND ANALOGS FROM INDUCING CYTOKINES |
| GB0001825D0 (en) * | 2000-01-26 | 2000-03-22 | Regen Therapeutics Plc | Peptides |
| WO2002013851A1 (en) * | 2000-08-17 | 2002-02-21 | The University Of Texas System | Use of colostrinin, constituent peptides thereof, and analogs thereof to promote neural cell differentiation |
| AU2000267883A1 (en) * | 2000-08-17 | 2002-02-25 | Regen Therapeutics Plc | Use of colostrinin, constituent peptides thereof, and analogs thereof for inducing cytokines |
| WO2002013850A1 (en) * | 2000-08-17 | 2002-02-21 | The University Of Texas System | Use of colostrinin, constituent peptides thereof, and analogs thereof as oxidative stress regulators |
| GB0029777D0 (en) * | 2000-12-06 | 2001-01-17 | Regen Therapeutics Plc | Peptides |
| HUP0200172A2 (hu) * | 2002-01-15 | 2003-11-28 | András Bertha | Eljárás tumorellenes hatóanyag kinyerésére |
| US20050042300A1 (en) * | 2002-10-22 | 2005-02-24 | Istvan Boldogh | Use of colostrinin, constituent peptides thereof, and analogs thereof as inhibitors of apoptosis and other cellular damage |
| AU2004220313B2 (en) * | 2003-03-11 | 2011-06-02 | Regen Therapeutics Plc | Purification of peptides from colostrum |
| CN1313487C (zh) * | 2003-06-10 | 2007-05-02 | 天津商学院 | 具有抗菌作用的免疫活性肽(Trpi) |
| US7547770B2 (en) * | 2003-11-03 | 2009-06-16 | Advanced Protein Systems | Colostral fractionation process |
| EP1723951A1 (en) * | 2005-04-21 | 2006-11-22 | N.V. Nutricia | Nutritional supplement with oligosaccharides for a category of HIV patients |
| US20070212367A1 (en) * | 2006-03-13 | 2007-09-13 | Keech Andrew M | Novel immunologically active peptide fragments of a proline-rich polypeptide isolated from colostral mammalian fluids for treatment of viral and non-viral diseases or diseased conditions |
| GB2436328A (en) * | 2006-03-22 | 2007-09-26 | Regen Therapeutics Plc | Peptide derived from colostrinin |
| US20110098216A1 (en) * | 2009-10-22 | 2011-04-28 | Regen Therapeutics Plc | Therapeutic uses of colostrinin |
| ITMI20111460A1 (it) * | 2011-07-29 | 2013-01-30 | Bionest Ltd | Composizioni per la terapia adiuvante dell'anoressia comprendenti anticorpi, fattori di crescita e citochine isolati dal colostro dei mammiferi |
| ITMI20112433A1 (it) * | 2011-12-30 | 2013-07-01 | Bionest Ltd | Composizioni per la terapia orale adiuvante dell'anoressia comprendenti anticorpi, antibatterici, fattori di crescita e citochine |
| EP2797609B1 (en) | 2011-12-30 | 2016-10-05 | Innomed S.A. | Combination of growth factors, cytokines, antibacterial/antiviral factors, stem cell stimulating factors, complement proteins c3a/c4a, immunoglobulins and chemotactic factors |
| EP2797610A1 (en) | 2011-12-30 | 2014-11-05 | BIONEST Ltd. | Combination of growth factors, cytokines, antibacterial/antiviral factors, stem cell stimulating factors, complement proteins c3a/c4a, and chemotactic factors |
| GB201205856D0 (en) | 2012-04-02 | 2012-05-16 | Randall Jeremy A P | Food supplement to support brain function |
| PL235821B1 (pl) * | 2014-11-04 | 2020-11-02 | Geo Poland Spolka Z Ograniczona Odpowiedzialnoscia | Wysokoprolinowy kompleks peptydowy do zastosowania w profilaktyce i wspomaganiu leczenia zaburzeń i stanów wymagających podwyższania i/lub modulacji poziomu neurotropowego czynnika pochodzenia mózgowego jako oznaczonego w osoczu krwi biomarkera i zawierający go preparat |
| US10621688B2 (en) | 2015-01-30 | 2020-04-14 | Hewlett-Packard Development Company, L.P. | M-ary cyclic coding |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ATE90569T1 (de) | 1988-04-19 | 1993-07-15 | Biotest Pharma Gmbh | Praeparat mit antikoerperaktivitaet und breitem wirkungsspektrum, daraus bestehende oder diese enthaltende mittel und deren verwendung zur behandlung von bakteriell oder toxin-bedingten erkrankungen und zur bekaempfung von protozoen. |
| JPH05163160A (ja) * | 1991-12-13 | 1993-06-29 | Snow Brand Milk Prod Co Ltd | 免疫低下に伴う感染症の予防及び治療用栄養剤 |
| JP3174611B2 (ja) * | 1992-02-28 | 2001-06-11 | 明治乳業株式会社 | 免疫賦活組成物 |
| US5645834A (en) | 1992-08-28 | 1997-07-08 | Immuno-Dynamics, Inc. | Method and product for treating failure of passive transfer and improving milk production in bovine species |
| GB9318611D0 (en) * | 1993-09-08 | 1993-10-27 | Sandoz Nutrition Ltd | Improvements in or relating to organic compounds |
| DE4337654C2 (de) | 1993-11-04 | 1996-08-08 | Biotest Pharma Gmbh | Verwendung boviner Kolostralmilch von nicht mit Viren hyperimmunisierten Tieren als Leberschutzpräparat |
| JP4112021B2 (ja) * | 1994-02-16 | 2008-07-02 | 明治乳業株式会社 | 乳酸菌を用いた免疫賦活剤 |
| AU6641896A (en) | 1995-08-07 | 1997-03-05 | New England Medical Center Hospitals, Inc., The | Infant formula and infant formula additives |
| DE19619990A1 (de) | 1996-05-17 | 1997-11-20 | Charlotte Adler | Verfahren zur Herstellung von Kolostralmilchprodukten sowie deren Verwendung |
| PL185442B1 (pl) | 1996-10-03 | 2003-05-30 | Georgiades Biotech Ltd | Środek farmaceutyczny o działaniu immunologicznym i psychotropowym, jego postać terapeutyczna oraz zastosowanie |
-
1996
- 1996-10-03 PL PL96316416A patent/PL185442B1/pl not_active IP Right Cessation
-
1997
- 1997-10-03 RU RU99109093/15A patent/RU2217152C2/ru not_active IP Right Cessation
- 1997-10-03 KR KR10-1999-7002904A patent/KR100508764B1/ko not_active IP Right Cessation
- 1997-10-03 JP JP10516329A patent/JP2001501929A/ja active Pending
- 1997-10-03 KR KR1020057004215A patent/KR20050046766A/ko not_active Application Discontinuation
- 1997-10-03 CN CNA031466095A patent/CN1535722A/zh active Pending
- 1997-10-03 AU AU45651/97A patent/AU4565197A/en not_active Abandoned
- 1997-10-03 IL IL12921197A patent/IL129211A/en not_active IP Right Cessation
- 1997-10-03 BR BR9712259-9A patent/BR9712259A/pt not_active Application Discontinuation
- 1997-10-03 US US09/269,845 patent/US6852700B1/en not_active Expired - Lifetime
- 1997-10-03 AR ARP970104585A patent/AR013612A1/es unknown
- 1997-10-03 GB GB9908331A patent/GB2333453B/en not_active Expired - Fee Related
- 1997-10-03 TR TR1999/01022T patent/TR199901022T2/xx unknown
- 1997-10-03 CA CA2266859A patent/CA2266859C/en not_active Expired - Fee Related
- 1997-10-03 EP EP97944005A patent/EP0932623A1/en not_active Withdrawn
- 1997-10-03 ZA ZA9708885A patent/ZA978885B/xx unknown
- 1997-10-03 HU HU9904368A patent/HUP9904368A3/hu unknown
- 1997-10-03 WO PCT/GB1997/002721 patent/WO1998014473A1/en active IP Right Grant
- 1997-10-03 CZ CZ0114999A patent/CZ298215B6/cs not_active IP Right Cessation
- 1997-10-03 CN CN97198535A patent/CN1131712C/zh not_active Expired - Fee Related
-
2004
- 2004-12-03 US US11/003,854 patent/US20050152985A1/en not_active Abandoned
-
2008
- 2008-02-13 JP JP2008031513A patent/JP2008174561A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| US20050152985A1 (en) | 2005-07-14 |
| JP2008174561A (ja) | 2008-07-31 |
| HUP9904368A3 (en) | 2000-07-28 |
| AU4565197A (en) | 1998-04-24 |
| GB2333453A (en) | 1999-07-28 |
| GB2333453B (en) | 2001-05-30 |
| GB2333453A8 (en) | 2000-11-27 |
| CZ114999A3 (cs) | 2000-06-14 |
| PL185442B1 (pl) | 2003-05-30 |
| EP0932623A1 (en) | 1999-08-04 |
| HUP9904368A2 (hu) | 2000-06-28 |
| IL129211A0 (en) | 2000-02-17 |
| KR20000048886A (ko) | 2000-07-25 |
| CN1535722A (zh) | 2004-10-13 |
| TR199901022T2 (xx) | 1999-07-21 |
| WO1998014473A1 (en) | 1998-04-09 |
| ZA978885B (en) | 1999-07-26 |
| CN1238782A (zh) | 1999-12-15 |
| KR20050046766A (ko) | 2005-05-18 |
| CZ298215B6 (cs) | 2007-07-25 |
| RU2217152C2 (ru) | 2003-11-27 |
| BR9712259A (pt) | 2000-01-25 |
| AR013612A1 (es) | 2001-01-10 |
| JP2001501929A (ja) | 2001-02-13 |
| US6852700B1 (en) | 2005-02-08 |
| KR100508764B1 (ko) | 2005-08-17 |
| CA2266859C (en) | 2012-05-08 |
| PL316416A1 (en) | 1998-04-14 |
| GB9908331D0 (en) | 1999-06-09 |
| CA2266859A1 (en) | 1998-04-09 |
| IL129211A (en) | 2004-08-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN1131712C (zh) | 初乳肽及其用途 | |
| EP0396616B1 (en) | Reduction of side effects of cancer therapy | |
| CN1468108A (zh) | 衍生自乳的骨保健组合物 | |
| FR2537436A1 (fr) | Procede de regulation de l'appetit et de l'efficacite de l'utilisation des aliments utilisant de l'interferon | |
| CN1146576C (zh) | 得自哺乳动物肝脏的蛋白质及其在肿瘤学中的应用 | |
| CN101054408A (zh) | 家蝇分泌型抗菌肽的分离方法及其产品和应用 | |
| CN1158856A (zh) | 能够针对人胃癌诱导免疫应答的肽和含该肽的预防或治疗人胃癌的药剂 | |
| CN1195544C (zh) | 用于慢性肝炎的肝功能改善剂 | |
| US9249188B2 (en) | Mammalian colostrum derived nanopeptides for broadspectrum viral and recurrent infections with a method of isolation thereof | |
| EP1375513A1 (en) | Immunopotentiators | |
| AU761148B2 (en) | Colostrinin, and uses thereof | |
| GB2352176A (en) | Colostrinin and uses thereof | |
| PL195627B1 (pl) | Zastosowania kolostryniny, kompozycje farmaceutyczne do leczenia przewlekłych chorób ośrodkowego układu nerwowego lub immunostymulacji i zastosowanie nonapeptydu | |
| MXPA99003108A (en) | Colostrinin, and uses thereof | |
| CN103393721A (zh) | 复合特异性转移因子制备工艺及医药用途 | |
| CN1395490A (zh) | 抗原特异性lgE抗体产生抑制剂 | |
| JPH08231589A (ja) | 新規なペプチドおよび免疫賦活剤 | |
| JPS5889195A (ja) | 標的細胞障害性因子の製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| C17 | Cessation of patent right | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 20031224 Termination date: 20131003 |